Getting back to serious things
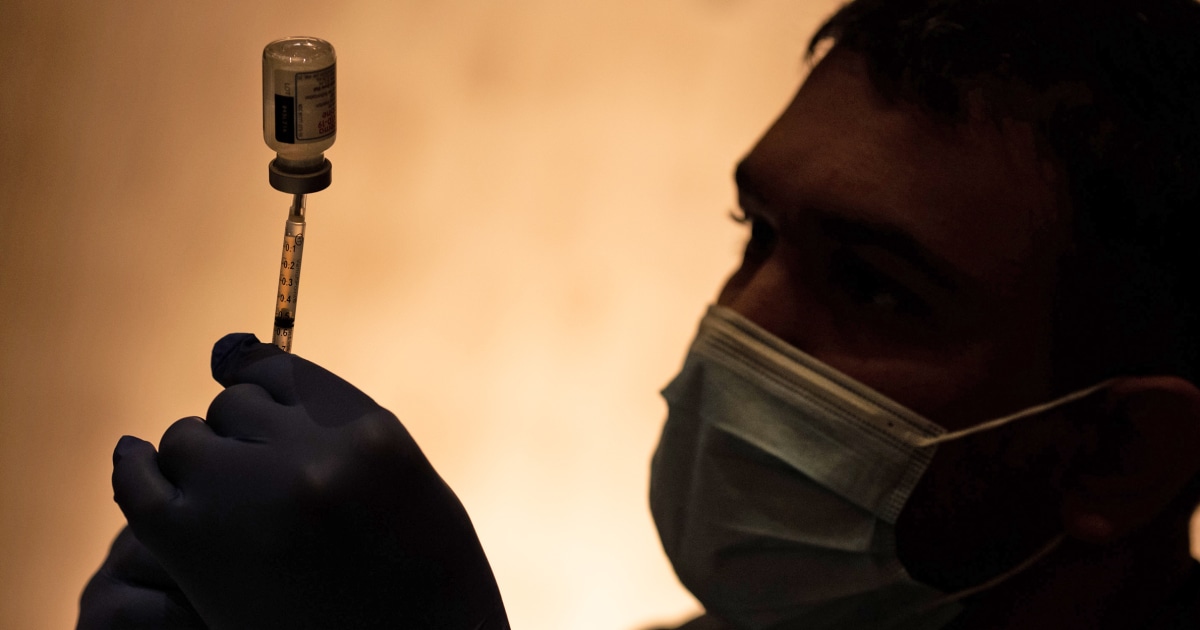
The US Food and Drug Administration on Wednesday authorized updated Covid-19 vaccine booster shots from Moderna and Pfizer. This is the first time updated Covid-19 vaccines have received emergency use authorization in the United States.
Both are bivalent vaccines that combine the companies' original vaccine with one that targets the BA.4 and BA.5 Omicron sublineages. Both companies submitted applications to the FDA for emergency use authorization for their updated vaccines last week.
The US Food and Drug Administration on Wednesday authorized updated Covid-19 vaccine booster shots from Moderna and Pfizer. This is the first time updated Covid-19 vaccines have received emergency use authorization in the United States.
Both are bivalent vaccines that combine the companies' original vaccine with one that targets the BA.4 and BA.5 Omicron sublineages. Both companies submitted applications to the FDA for emergency use authorization for their updated vaccines last week.